
La invención de las técnicas de manipulación del ADN, el libro de instrucciones de la vida, ha supuesto una revolución científica sin precedentes. El ser humano dispone de herramientas para alterar el genoma de los seres vivos, diseñando microorganismos, plantas y animales a medida, con fines diversos (producir fármacos, mejorar la producción, obtener órganos para trasplantes y un largo etcétera de aplicaciones); con esas mismas técnicas se puede manipular el genoma de nuestra propia especie.
Herramientas como CRISPR-Cas9, permiten editar de manera sencilla y poco costosa el genoma, buscar la secuencia que se desea modificar y eliminarla o sustituirla por la correcta, libre de mutaciones indeseadas. La edición de genes abre nuevas expectativas terapéuticas: corregir enfermedades en su origen, modificando los genes que las causan; pero también abre muchas incógnitas sobre los límites de la manipulación genética.
1. CONCEPTO DE BIOTECNOLOGÍA
La biotecnología consiste en la utilización de las propiedades y los componentes de los seres vivos para fines prácticos e industriales. Utiliza tanto seres vivos (animales, plantas y microorganismos) como sus componentes: células y biomoléculas (enzimas, proteínas, ácidos nucleicos, etc).
Los organismos vivos han adquirido a través de la evolución propiedades que el ser humano ha intentado aprovechar a lo largo de la historia.
El término biotecnología se atribuye al ingeniero agrícola Karl Ereky en 1919.
En 1992, el Convenio sobre la Diversidad Biológica definió la bioteconología como cualquier aplicación, sustentada en procesos científicos y técnicos, que utilice, en alguna de sus etapas, organismos vivos o sus derivados para crear o modificar productos o procesos útiles para los humanos.
Podemos diferenciar entre biotecnología tradicional, con miles de años de antigüedad, y biotecnología moderna, que emplea las técnicas de la ingeniería genética y surge a partir de 1970, con el descubrimiento de la tecnología del ADN recombinante.
1.1 La biotecnología tradicional
El origen de la biotecnología tradicional podemos situarlo unos 10 000 años atrás, con el inicio de la domesticación de plantas y animales a través de la selección artificial. A lo largo de los siglos, se han seleccionado determinadas características y se han realizado cruces entre las variedades más exitosas.
La biotecnología tradicional utiliza los microorganismos para la obtención de productos útiles, tanto en la producción de alimentos como en la de antibióticos. Mediante las fermentaciones se obtienen derivados lácteos, pan y bebidas alcohólicas como vino, cerveza, sidra o sake, dependiendo del sustrato empleado.
2. TÉCNICAS DE INGENIERÍA GENÉTICA
A continuación, analizaremos algunas de las herramientas que utiliza la ingeniería genética.
2.1 Tecnología del ADN recombinante
El ADN recombinante es una molécula de ADN formada por la unión de dos fragmentos de distinto origen: el gen que interesa clonar (inserto) y una molécula de ADN que actúa como transportadora (vector) para introducir el gen en las células hospedadoras.

El descubrimiento en los años 70 de las enzimas de restricción presentes en bacterias, hizo posible esta tecnología.
A. Enzimas de restricción: las tijeras moleculares
Las enzimas de restricción son endonucleasas, es decir, enzimas capaces de romper los enlaces fosfodiéster entre los nucleótidos.
Su utilidad deriva de su gran especificidad: reconocen secuencias de ADN concretas, de 4 a 8 bases, denominadas sitios de reconocimiento o de restricción.
Hay diferentes endonucleasas de restricción, producidas por distintas bacterias, en las que actúan como mecanismo de defensa contra virus bacteriófagos. Cuando la bacteria detecta la entrada de ADN de un fago, lo degrada utilizando sus enzimas de restricción a modo de tijeras moleculares. Las bacterias protegen su propio ADN de la acción de estas enzimas mediante la metilación de bases en los sitios de restricción, inmediatamente después de la división celular.
Los sitios de restricción suelen ser secuencias palindrómicas y actúan como dianas para las enzimas de restricción. Estas cortan las dos cadenas y pueden dejar dos tipos de extremos: extremos romos o bien extremos cohesivos o pegajosos.
Si el corte se produce justo en el centro de simetría de la secuencia palindrómica, los fragmentos resultantes presentan extremos romos.
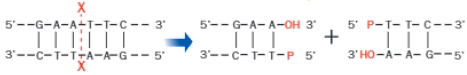
Si el corte se produce escalonado, se generan extremos con bases desapareadas, denominados extremos cohesivos.
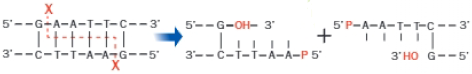
En condiciones apropiadas, dos moléculas de ADN cortadas con la misma enzima de restricción, que deje extremos cohesivos, pueden unirse de modo permanente, al interaccionar y aparearse las bases de sus extremos, añadiendo la enzima ADN ligasa, que cataliza la formación del enlace fosfodiéster.
La tecnología del ADN recombinante emplea los siguientes materiales:
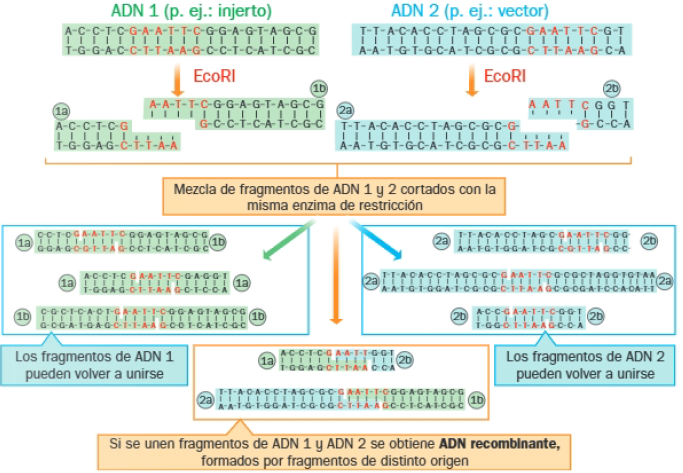
- Inserto: gen de interés que se desea clonar.
- Vector de clonación: molécula de ADN a la que se une el inserto y que facilita su entrada en las células hospedadoras y la posterior replicación.
- Enzimas de restricción: con las que cortar el inserto y el vector, de modo que queden ambos con extremos cohesivos.
- Enzima ADN ligasa: une definitivamente el vector y el inserto.
- Células hospedadoras: en las que se producirá la replicación del ADN recombinante.
B. Procedimiento de clonación celular de ADN mediante la tecnología del ADN recombinante.
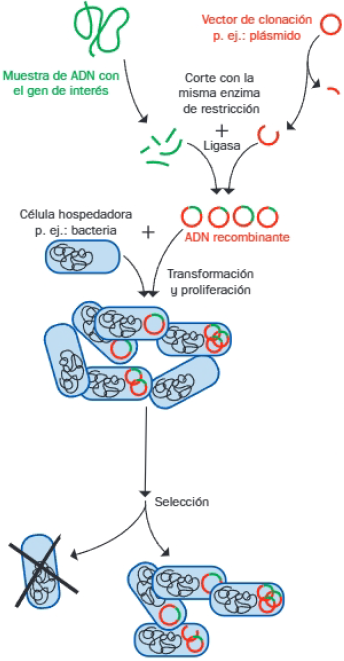
- 1ª etapa. Preparación del vector y del gen de interés: Como vector de clonación pueden utilizarse plásmidos, cósmidos, genomas víricos, etc.
- 2ª etapa. Formación del ADN recombinante: Inserto+vector se unen mediante ligasa.
- 3ª etapa. Introducción en células hospedadoras: El ADN recombinante se introduce en células hospedadoras con el fin de que se replique en ellas.
- 4ª etapa. Replicación del ADN recombinante: El vector tiene capacidad de replicación independiente; aumenta el número de copias.
- 5ª etapa. Proliferación celular: Las células se cultivan en un medio adecuado.
- 6ª etapa. Selección: Se seleccionan las células que han incorporado el ADN recombinante.
- 7ª etapa. Expresión del gen: Es opcional, si la finalidad de la clonación es la obtención de la proteína codificada por el inserto.
Los vectores de clonación y las células hospedadoras deben poseer unas características específicas.
Vectores de clonación
Los vectores son moléculas pequeñas de ADN cuya misión es transportar el gen que se desea clonar hasta la célula hospedadora, favoreciendo su replicación dentro de la misma.
Los vectores de clonación deben tener tres componentes esenciales:
- Un origen de replicación: deben tener capacidad para replicarse de modo independiente del genoma de la célula hospedadora.
- Uno o más genes marcadores que permitan seleccionar fácilmente las células hospedadoras que han incorporado el ADN recombinante.
- Al menos, un sitio de restricción.
Tipos de vectores de clonación
- Plásmidos
- Los plásmidos son moléculas de ADN circular de doble cadena, extracromosómico, presentes en las bacterias, que se replican independientemente del cromosoma principal; puede haber múltiples copias en una célula.
Presentan genes de resistencia a antibióticos que actúan como marcadores y facilitan la detección y selección de los clones que los contienen. En la naturaleza, se transmiten de una bacteria a otra por conjugación; en el laboratorio, pueden introducirse en las bacterias por transformación, mediante choque de calor o por electroporación.
Los primeros utilizados fueron plásmidos naturales, posteriormente se han sintetizado in vitro con las características deseables.
- Los plásmidos son moléculas de ADN circular de doble cadena, extracromosómico, presentes en las bacterias, que se replican independientemente del cromosoma principal; puede haber múltiples copias en una célula.
- Bacteriófagos o fagos
- Son virus que parasitan a bacterias. Se utilizan cuando el fragmento de ADN que se quiere clonar es de mayor tamaño que el que puede transportar un plásmido.
Los fagos como vectores tienen como ventajas que pueden llevar insertos de mayor tamaño que los plásmidos y que son mucho más eficientes penetrando en las células hospedadoras.
- Son virus que parasitan a bacterias. Se utilizan cuando el fragmento de ADN que se quiere clonar es de mayor tamaño que el que puede transportar un plásmido.
- Cósmidos
- Son vectores sintéticos que combinan las ventajas de los plásmidos y del fago gamma.
- Cromosomas artificales
- Permiten clonar grandes segmentos de ADN eucariota.
Células hospedadoras
Deben ser de crecimiento rápido, no ser patógenas y favorecer la entrada del ADN recombinante. Las más utilizadas son células procariotas como Escherichia coli o Bacillus subtilis, o bien células eucariotas la levadura Saccharomyces cerevisiae.
2.2 Separación de fragmentos de ADN mediante electroforesis en gel
La electroforesis es una técnica de separación de moléculas en función de su movilidad, sometidas a una campo eléctrico.
El ADN presenta cargas negativas en los grupos fosfato que están ionizados; por tanto, fragmentos de ADN sometidos a un campo eléctrico migran hacia el polo positivo.
La electroforesis se realiza sobre diferentes soportes, pero el más común es el gel de agarosa.
La agarosa es un polisacárido que, en disoluciones entre 0,5-2%, forma un gel semisólido constituido por una matriz o trama tridimensional que ofrece resistencia al avance de las moléculas; los fragmentos de ADN de menos tamaño se desplazan con más rapidez, por lo que la electroforesis separa los fragmentos de ácido nucleico según su tamaño o longitud.
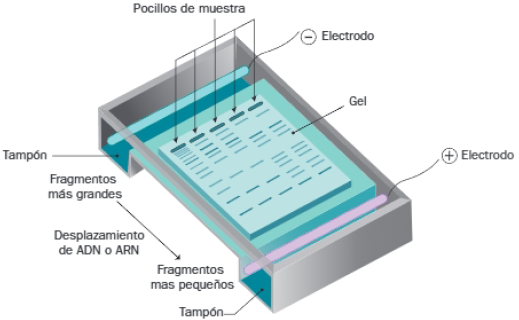
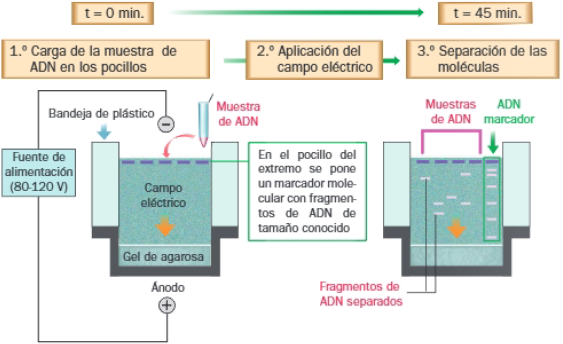
Se utilizan marcadores moleculares, mezclas de fragmentos de ADN de tamaño conocido, a partir de los que se puede deducir el tamaño de los fragmentos de la muestra.
2.3 Hibridación de ácidos nucleicos
El fundamento de la hibridación es la renaturalización de cadenas de ADN previamente desnaturalizado mediante calor.
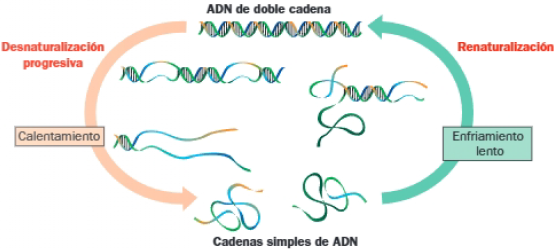
La hibridación es el proceso de formación de moléculas de ADN dúplex con dos cadenas de diferente origen, o ADN híbrido. Tiene lugar cuando dos cadenas complementarias se ponen en contacto. También puede darse entre una cadena de ADN y una de ARN complementarias.
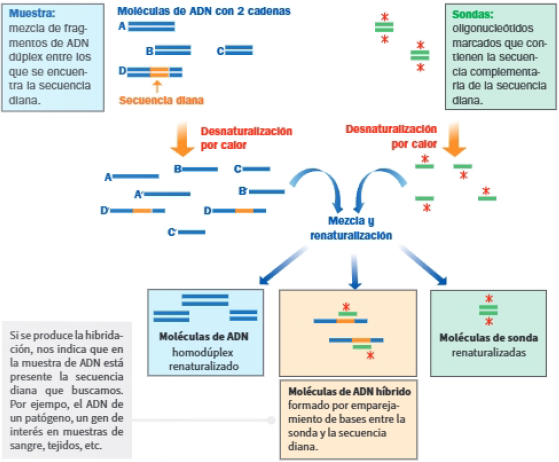
La hibridación se emplea para identificar en una muestra de ADN una secuencia de nucleótidos conocida, denominada secuencia diana. Para localizar la secuencia diana se utiliza una sonda: fragmento de ADN marcado que contiene la secuencia complementaria de la secuencia diana.
El procedimiento se muestra a continuación:
2.4 Reacción en cadena de la polimerasa
La PCR es una técnica de amplificación del ADN in vitro, un método de clonación acelular de moléculas de ADN.
La reacción en cadena de la polimerasa (PCR) es una técnica desarrollada en los años 80 del siglo XX por Kary Mullis, que recibió el Premio Nobel de Química en 1993. Su objetivo es conseguir múltiples copias de un gen o de un fragmento de ADN.
Clonar: hacer copias genéticamente idénticas de un elemento precursor.

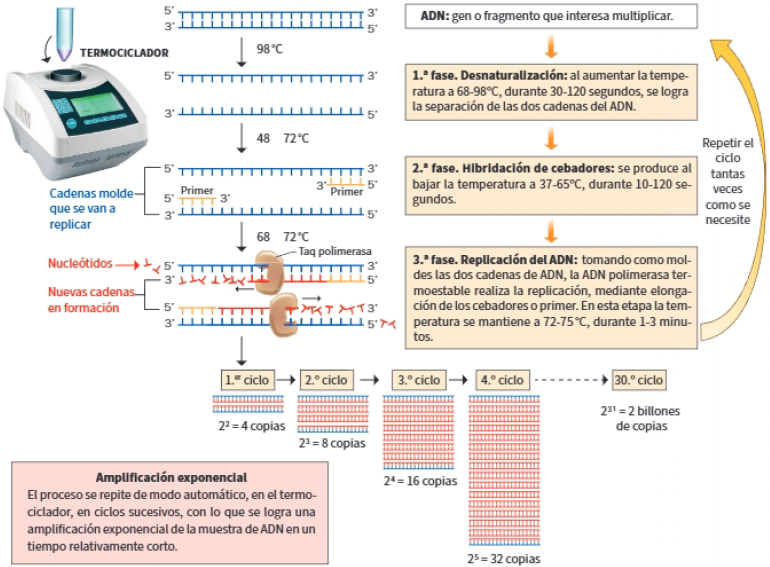
Fundamento: realizar ciclos de replicación del ADN sucesivos.
Material necesario: ADN de interés que se desea replicar, cebadores primers; nucleótidos trifosfato de A, T, C y G, ADN polimerasa termoestable, que soporte altas temperaturas.
Procedimiento: cada ciclo consta de 3 fases: desnaturalización del ADN por calor, unión de los cebadores y replicación del ADN, tal y como veremos ahora en la siguiente imagen:
2.5 Retrotranscripción
La retrotranscriptasa o RT permite obtener ADN, denominado ADNc o ADN complementario, a partir de una molécula de ARN que actúa como molde para la transcriptasa inversa o reversotranscriptasa.
La enzima transcriptasa inversa presente en los retrovirus sintetiza ADN tomando ARN como molde.
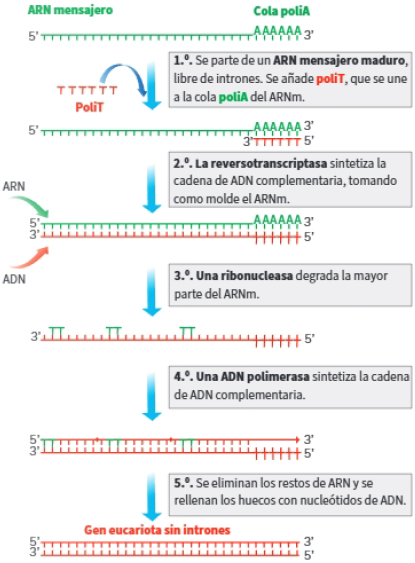
Mediante la transcripción inversa se pueden obtener genes eucariotas libres de intrones, por ejemplo, el gen de la insulina, para transferirlo a bacterias que lo expresen y produzcan la hormona humana.
En los virus con ARN como material genético, permite obtener ADN complementario del genoma vírico para procesos posteriores, como la PCR.
2.6 Genotecas, las bibliotecas de ADN
Una genoteca o biblioteca de ADN es una colección de fragmentos de ADN clonados.
Existen dos tipos diferentes de genotecas:
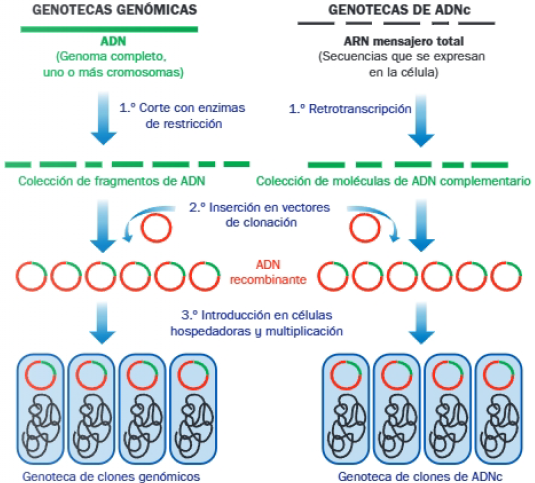
- Genotecas genómicas: representan en su conjunto el ADN total de un organismo de interés. Incluyen todas las secuencias, las que se expresan y las que no.
- Genotecas de ADNc: representan el conjunto de genes que se están expresando en un órgano o tejido determinado o en una situación particular o instante del crecimiento o desarrollo. El primer paso de la construcción de una genoteca de ADNc consiste en el aislamiento del ARN mensajero, que se diferencia con facilidad por la cola poliA en el extremo 3′. Mediante la transcriptasa reserva, se obtiene el ADNc.
Las genotecas tienen múltiples aplicaciones, tales como:
- Conservación de muestras del genoma de organismos para estudios posteriores.
- Aislamiento de genes y secuencias determinadas implicados en patologías.
- Punto de partida para la búsqueda de genes que son sometidos posteriormente a procesos de clonación, secuenciación, expresión, etc., para su estudio.
Como veremos más adelante, el desarrollo en las últimas décadas de los métodos de secuenciación de nueva generación, ha permitido prescindir de la producción previa de las genotecas.
2.7 Secuenciación del ADN
La secuenciación del ADN consiste en determinar la secuencia de nucleótidos de un fragmento de ADN. En ocasiones, también pueden secuenciarse el ARN.
Se distinguen dos tipos de técnicas de secuenciación:
- Secuenciación de 1ª generación o método de Sanger: Se fundamenta en el uso de ddNTP (didesoxinucleótidos trifosfato). Permite secuenciar un gen concreto y continúa siendo la técnica que ofrece mayor fiabilidad.
- Secuenciación de nueva generación (NGS): También se denominan técnicas masivas o paralelas, porque permiten secuenciar una gran cantidad de fragmentos de ADN de modo paralelo y en muy poco tiempo.
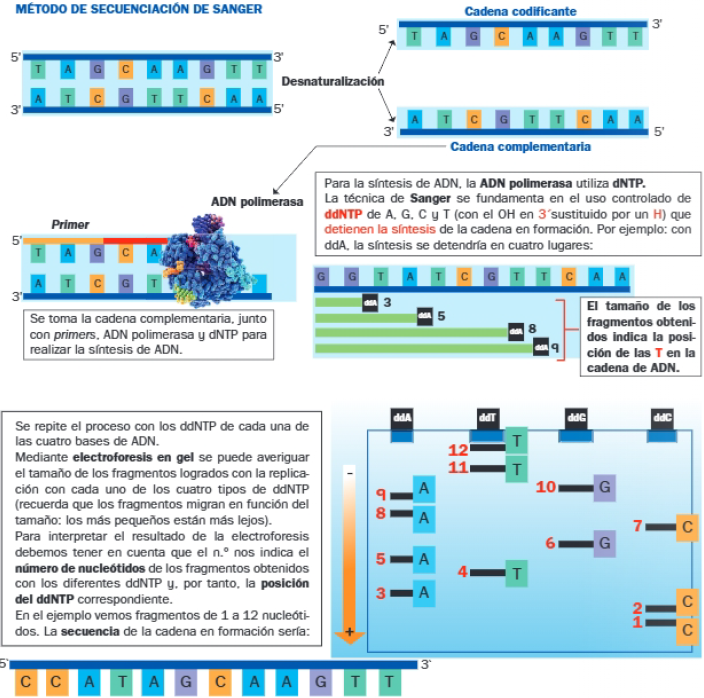
A. Técnica de secuenciación de Sanger
El fundamento básico de esta técnica se muestra en el siguiente esquema:
B. Técnicas de secuenciación de nueva generación
Las técnicas de secuenciación de nueva generación (NGS) tienen en común una serie de pasos:
- Corte del ADN de la muestra en varios fragmentos.
- Marcaje del ADN por medio de primers que señalan el punto de inicio de la replicación.
- Amplificación mediante PCR.
- Secuenciación o lectura de los fragmentos de ADN.
- Reconstrucción de la secuencia completa y almacenamiento de datos.
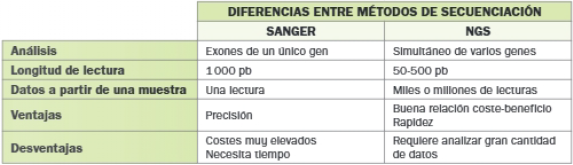
La técnica de Sanger continúa siendo apropiada para secuenciar un único gen, dada su alta fiabilidad; las NGS se utilizan cuando se necesita secuenciar mayor cantidad de ADN.
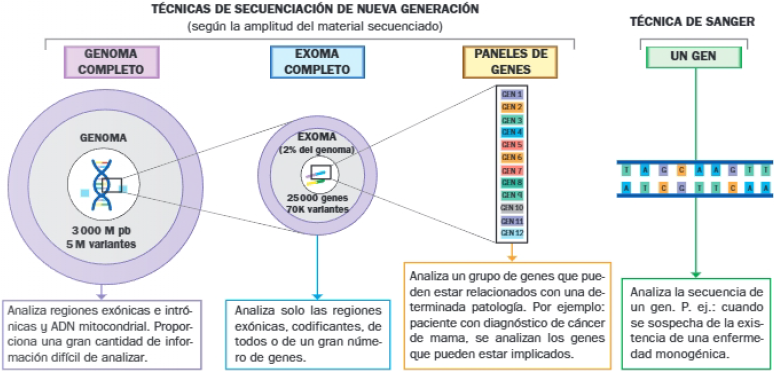
2.8 CRISPR-Cas: editando genes
En 2001, Francisco Mojica, microbiólogo y profesor en la Universidad de Alicante, acuñó el término CRISPR, para referirse a repeticiones palindrómicas cortas agrupadas y regularmente interespaciadas presentes en el ADN de las bacterias; en estas, forma parte de un sistema defensivo natural contra las infecciones víricas.
Cuando un virus infecta a una bacteria, le inyecta su ADN; la bacteria, que responde produciendo enzimas Cas para cortar en trozos el ADN vírico, lo fragmenta e incorpora los fragmentos de su genoma; pero no lo hace al azar, sino entre las secuencias CRISPR. Posteriormente, los fragmentos de ADN viral se transcriben y se obtienen ARNs que las proteínas Cas usan como guías para identificar y degradar ácidos nucleicos virales en infecciones posteriores.
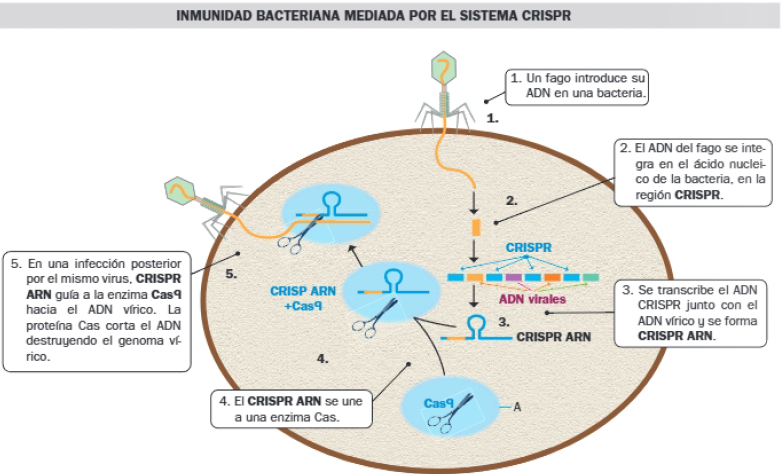
CRISPR es una técnica de edición génica que permite cortar el ADN en un sitio específico y editarlo; es decir, permite reescribir la secuencia de nucleótidos de cualquier gen. También se conoce como mutagénesis dirigida.
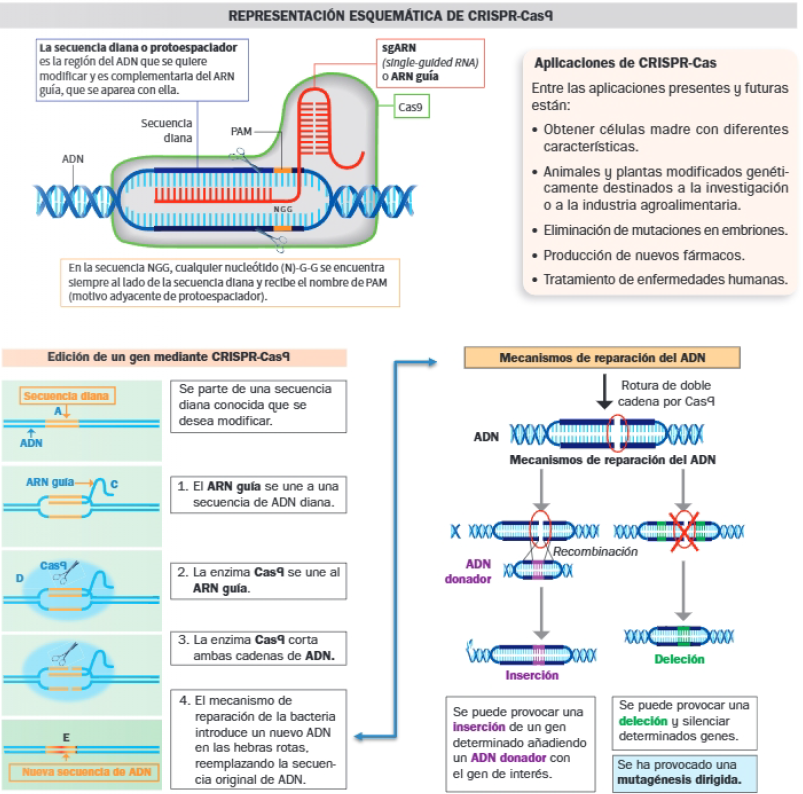
En 2012, los equipos de Jennifer Doudna y Emmanuelle Charpentler lograron una guía de ARN que conservaba un extremo que le permitía unirse a la proteína Cas9; el otro extremo lo modificaron, de modo que podían poner en él cualquier secuencia de interés, complementaria de una secuencia diana conocida. De este modo, CRISPR-Cas9 puede cortar de forma específica la secuencia diana elegida.
La edición de un gen mediante CRISPR-Cas9 puede hacerse directamente en el núcleo de las células vivas. Posteriormente, se ha logrado además insertar con éxito nuevas secuencias de ADN de forma precisa en el sitio de corte, reemplazando a la secuencia original; es decir, se ha logrado no solo cortar determinados genes, silenciándolos, sino también reescribirlos de forma correcta, eliminando los fallos que pudieran tener. Una ventaja que tiene sobre los sistemas, además de precisión, es que permite actuar sobre muchos genes a la vez.
Los sistemas CRISPR-Cas9 son muy diversos, ya que cada bacteria y cada arquea tienen el suyo propio: CRISPR-Cas9 es uno de los sistemas, el cual deriva de la bacteria Streptococcus pyogenes y está compuesto por la proteína Cas9 y un ARN guía que dirige a Cas9 al sitio diana.
3. APLICACIONES DE LA BIOTECNOLOGÍA
La biotecnología utiliza sistemas biológicos y organismos vivos -o derivados- para crear o modificar procesos o productos para usos específicos.
Las principales aplicaciones de la biotecnología se centran en 5 áreas: biosanitaria, agrícola, ambiental, industrial y marina; según el área de aplicación, se habla de:
- Biotecnología roja (Biomedicina): Con múltiples aplicaciones: obtención de fármacos, diagnóstico de enfermedades, elaboración de vacunas, terapia génica, terapias celulares (células madre), identidad molecular (medicina forense).
- Biotecnología verde: Aplicada a procesos agrícolas. Plantas genéticamente modificadas con tolerancia a condiciones adversas, mejores propiedades nutricionales, resistentes a herbicidas, plagas, etc.
- Biotecnología gris: Busca soluciones a problemas medioambientales, tales como la recuperación de ecosistemas naturales contaminados mediante procesos de biorremediación.
- Biotecnología blanca: Aplicada a procesos industriales. Desarrollo de nuevos materiales, como pueden ser los bioplásticos, biocombustibles, etc.
- Biotecnología azul: Aplicada a procesos relacionados con el mar, como pueden ser los productos para la acuicultura.
Muchas de estas aplicaciones se fundamentan en el uso de organismos genéticamente modificados (OGM). Dentro de los OGM debemos diferenciar:
- Organismos transgénicos: son aquellos a los que se les ha introducido algún gen de otra especie. Surgen a partir de la tecnología de ADN recombinante.
- Organismos cisgénicos: Se desarrollan a partir de la tecnología CRISPR-Cas9 que permite editar genes.
En las aplicaciones de los OGM, la legislación de la UE que las regula diferencia entre:
- Utilización confinada: los trabajos que se realizan en laboratorios, invernaderos y animalarios con microorganismos, plantas y animales a los que se modifica el material genético mediante la inserción o eliminación de genes.
- Utilización voluntaria: introducción deliberada en el medio ambiente de un organismo o una combinación de organismos modificados genéticamente.
- Comercialización: implica una entrega a terceros de OMG o de productos que los contengan. No se considera comercialización el suministro de OMG para las actividades de utilización confinada y/o liberación voluntaria con fines distintos a la comercialización.
En los dos primeros casos, en la UE, los Estados miembros son responsables de la evaluación de las solicitudes y, en su caso, de la autorización. En España, las autorizaciones las concede el Consejo Interministerial de OMG o los órganos competentes de las comunidades autónomas, previa autorización del riesgo por la Comisión Nacional de Bioseguridad. La autorización con fines comerciales la conceden las autoridades comunitarias competentes en el ámbito de la Unión Europea.
3.1 Aplicaciones en medicina
La denominada biotecnología roja analiza los procesos biológicos de células, bacterias u otros microorganismos, y los utiliza en el desarrollo de productos que ayuden en la prevención y el tratamiento de enfermedades. entre las aplicaciones desarrolladas actualmente, destacan las siguientes:
A. Obtención de fármacos
Se obtienen proteínas mediante la tecnología del ADN recombinante, a partir de organismos transgénicos para el tratamiento de distintas enfermedades, como puede ser la insulina humana producida por la E.coli para el tratamiento de la diabetes, así como para producirse antígenos, anticuerpos y vacunas. Veamos algunos ejemplos en la siguiente tabla:
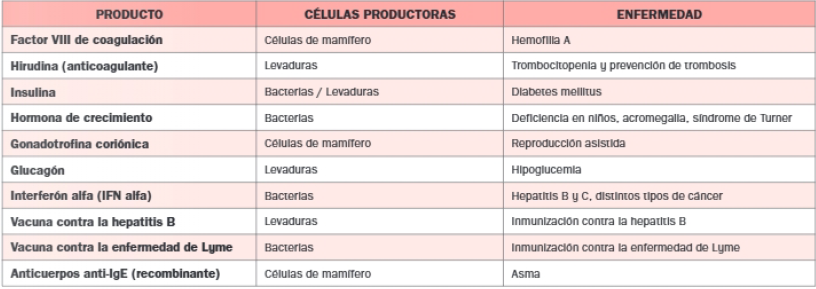
Y aquí podemos ver un ejemplo de una proteína humana mediante ADN recombinante:
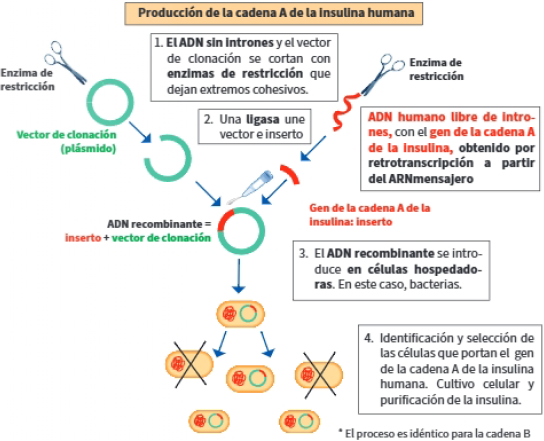
La insulina humana fue el primer fármaco comercializado, obtenido mediante la tecnología del ADN recombinante. La insulina está formada por dos cadenas polipeptídicas A y B. Es necesario clonar los genes en ambas cadenas, libres de intrones, en bacterias, para sintetizar la insulina.
B. Diagnóstico de enfermedades
La biotecnología ha permitido grandes avances en el diagnóstico de enfermedades, tanto en las de origen genético como en las causadas por microorganismos.
En relación con las de origen genético, se han identificado las causas genéticas de más de 3000 enfermedades. Detectar una mutación de riesgo, como en el caso del cáncer, ayudará a tomar medidas preventivas. Conocer las causas genéticas de enfermedades sirve también para prevenir su transmisión a la siguiente generación, recurriendo al consejo genético.
La secuenciación del ADN y la elaboración de bases de datos facilitan el diagnóstico. Se puede analizar la secuencia de un gen concreto si se sospecha de una enfermedad monogénica, de un panel de genes implicados en una determinada dolencia, el exoma de un paciente e incluso su genoma completo. Las nuevas tecnologías, como los microarrays o chips de ADN, han reducido los tiempos y abaratado los costes. El conocimiento del genoma y el proteoma humanos ha sido clave para detectar y tratar múltiples alteraciones.

C. Terapias con células madre
Las terapias celulares consisten en la introducción de nuevas células en un tejido.
Las células madre se caracterizan principalmente por su capacidad de división mediante mitosis y por ser células indiferenciadas. Al dividirse dan lugar a células hijas que pueden permanecer como células madre, o bien, iniciar el proceso de diferenciación para dar lugar a un tipo celular específico.
Según su origen, diferenciamos entre células madre embrionarias y adultas.
Las células madre pluripotentes inducidas (IPS) son células adultas modificadas genéticamente, sometidas a un proceso de desdiferenciación, para que se comporten como células madre embrionarias y recuperen la capacidad de formar todos los tipos de células.
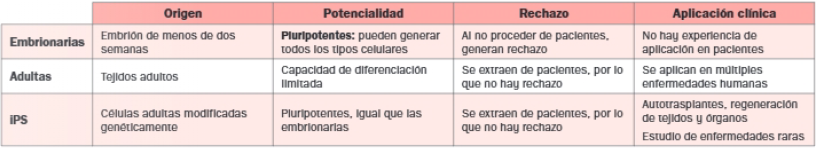
D. Terapia génica
La terapia génica consiste en introducir uno o más genes para tratar, prevenir o curar una enfermedad, como por ejemplo introduciendo formas sanas de un gen que está dañado, o reemplazarlo el gen defectuoso por una versión sana del mismo.
Hasta el desarrollo de la tecnología CRISPR, la terapia génica utilizada como vectores virus modificados, aprovechando su capacidad para seleccionar e introducir su material genético en las células diana. La terapia puede realizarse en vivo o ex vivo.
La edición génica mediante CRISPR-Cas9 presenta ventajas respecto a la tecnología anterior, tales como: gran facilidad de modificación, reducir la respuesta inmunitaria adversa y el riesgo de que se modifique el ADN en posiciones no deseadas.
E. Medicina forense
Las pruebas de ADN permiten la identificación de restos humanos en catástrofes, exhumaciones de fosas, escenas de crímenes, restos arqueológicos, etc. La PCR permite amplificar muestras muy pequeñas y disponer de material suficiente. También se utiliza el ADN en pruebas de paternidad, para determinar parentescos y en estudios evolutivos.
3.2 Aplicaciones en la industria agroalimentaria
El cultivo de organismos genéticamente modificados está ampliamente extendido actualmente.
La denominada biotecnología verde se emplea para mejorar la resistencia a determinadas plagas y enfermedades, la resistencia a herbicidas, mejorar las cualidades nutritivas, mayor tolerancia a factores ambientales adversos como la sequía, las heladas, etc.
3.3 Aplicaciones en la ganadería
En los animales modificados genéticamente se ha buscado mejorar la producción, la calidad de la carne o la leche, la resistencia a enfermedades, a condiciones ambientales adversas, etc.
También se producen animales transgénicos productores de fármacos o con determinadas mutaciones para servir de modelos en el estudio de enfermedades.
3.4 Aplicaciones en el medio ambiente
Entre las aplicaciones de la biotecnología al medio ambiente destaca la biorremediación.
La biorremediación puede definirse como un conjunto de procesos que utilizan organismos vivos (hongos, plantas, microorganismos) o enzimas derivadas de ellos, para la recuperación en entornos contaminados (tanto en agua como suelos o aire).
- La biorremediación microbiana utiliza microorganismos directamente en el foco de contaminación. Puede ser microorganismos propios del ecosistema o introducidos. Esta ayuda, entre otras cosas, a la eliminación de los vertidos de hidrocarburos que, con frecuencia, se producen en el mar. Los derrames de hidrocarburos tienen graves consecuencias sobre los ecosistemas a corto, medio y largo plazo.
- La fitorremediación utiliza plantas para eliminar contaminantes del suelo, etc.
- La rizofiltración utiliza la capacidad de filtrado de las raíces para eliminar sustancias tóxicas o exceso de nutrientes de aguas contaminadas. Emplea plantas cultivadas hidropónicamente, es decir, sin tierra.
- La degradación enzimática se utiliza para degradar sustancias nocivas.
3.5 Aplicaciones industriales
La biotecnología industrial tiene como objetivo optimizar los procesos industriales de diferentes sectores con el fin de obtener productos biodegradables, cuya producción requiera menos energía y genere menos residuos; de esta manera, se reduce el impacto medioambiental.
Algunas de las herramientas biotecnológicas utilizadas industrialmente son: las enzimas, los microorganismos, las líneas celulares, las fermentaciones, las materias primas de origen renovables y los productos biodegradables, entre otros. Actualmente, la biotecnología se aplica a sectores industriales como la cosmética, la alimentación, los combustibles y las sustancias químicas. Proporciona aditivos, detergentes, biocombustibles, bioplásticos, nuevos tejidos, etc.
4. MICROORGANISMOS Y BIOTECNOLOGÍA
El término microorganismo incluye a los seres vivos que, por su pequeño tamaño, resultan imperceptibles para el ojo humano y solo pueden verse con ayuda del microscopio. Los microorganismos se presentan como células aisladas o en colonias. Son microorganismos procariotas los dominios Archaea y Bacteria, y hay microorganismos eucariotas en los reinos Protoctista y Fungi. Con frecuencia, el término se usa para referirse a formas acelulares como virus, viroides y priones.
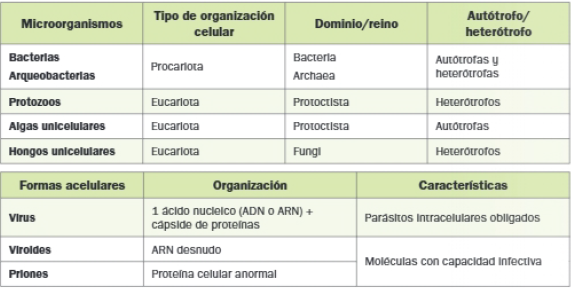
Gran parte de los procesos biotecnológicos se fundamentan en cualidades de los microorganismos, sobre todo de las bacterias y las arqueobacterias. La siguiente tabla recoge algunas de las aplicaciones que hemos visto:
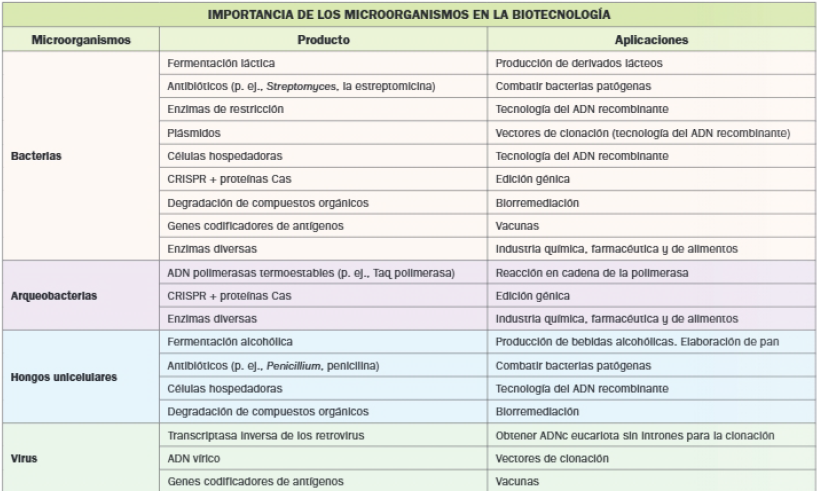
Fuente: Biología 2 (Mc Graw Hill).