CARACTERÍSTICAS GENERALES DE LAS PROTEÍNAS
Las proteínas son nutrientes fundamentales para el ser humano, ya que son las únicas que proporcionan nitrógeno.
Las proteínas o prótidos son biomoléculas orgánicas lineales, compuestas por carbono, oxígeno, hidrógeno y nitrógeno principalmente.
Se encuentran, en abundancia, en todos los seres vivos donde tienen una enorme importancia biológica, ya que desempeñan un gran número de funciones, además de ser moléculas específicas. Se forman por polimerización de monómeros de aminoácidos. Las largas cadenas de aminoácidos se pliegan en una gran diversidad de formas.
LOS AMINOÁCIDOS
Los aminoácidos son los constituyentes básicos de los péptidos y las proteínas. Y aunque se conocen como 200 diferentes, solo 20 son proteicos, están codificados en el ADN y son los mismos para todos los seres vivos.
Los aminoácidos no proteicos realizan importantes funciones específicas en el metabolismo: actúan como neurotransmisores , forman parte de vitaminas, son metabolitos intermediarios de la degradación de proteínas, etc.
La moléculas del aminoácido consta de un aminoácido central, llamado carbono alfa, al que se le une un hidrógeno, un grupo carboxilo, un grupo amino y un radical, que es distinto en cada aminoácido.
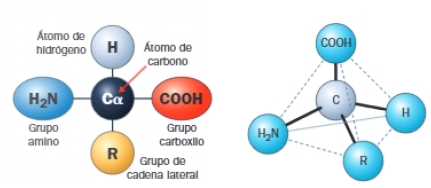
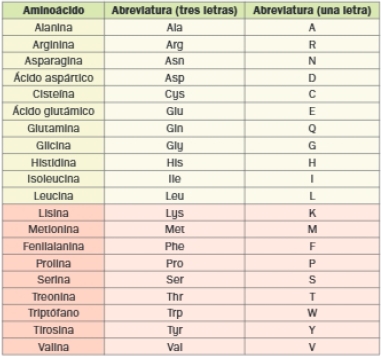
Todos los aminoácidos proteicos tienen el grupo amino y el grupo carboxilo sobre un mismo carbono, así que son por tanto alfa-aminoácidos. Como ya hemos indicado, el Carbono alfa completa sus cuatro sustituyentes con un átomo de hidrógeno y un radical orgánico que forma la cadena lateral. Los aminoácidos proteicos tienen dos sistemas de nomenclatura, que es la clásica (3 letras) y la actual (1 letra).
Clasificación de los aminoácidos
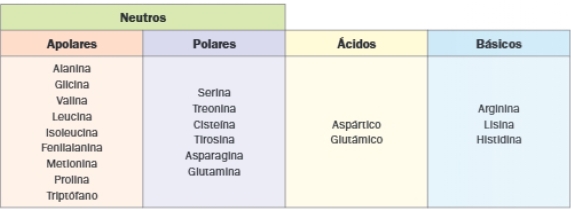
Los aminoácidos se clasifican según su grupo radical en los siguientes:
- Aminoácidos neutros: en sus cadenas laterales no presentan ni grupos carboxilo ni grupo amino, por lo que su carga neta es 0 a pH neutro. Aquí encontramos a los aminoácidos neutros polares y apolares.
- Aminoácidos ácidos: tienen en su cabeza lateral un segundo grupo carboxilo que les confiere carga negativa y características ácidas.
- Aminoácidos básicos: tiene en su cadena lateral un grupo amino que les confiere carga positiva y características básicas.
También podríamos clasificarlos en función de su obtención y requerimiento es la siguiente:
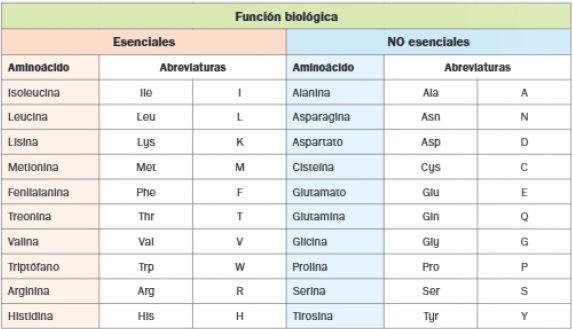
- Aminoácidos esenciales: son aquellos que nuestro cuerpo no sintetiza y debemos ingerir en la dieta.
- Aminoácidos no esenciales: nuestro organismo los puede producir.
- Aminoácidos condicionales: por lo general, no son esenciales excepto en momentos de enfermedad o estrés o en niños muy pequeños, ya que sus requerimientos son mayores que su capacidad para sintetizarlos.
Por último, según su cadena lateral, podríamos hacer una tercera clasificación:
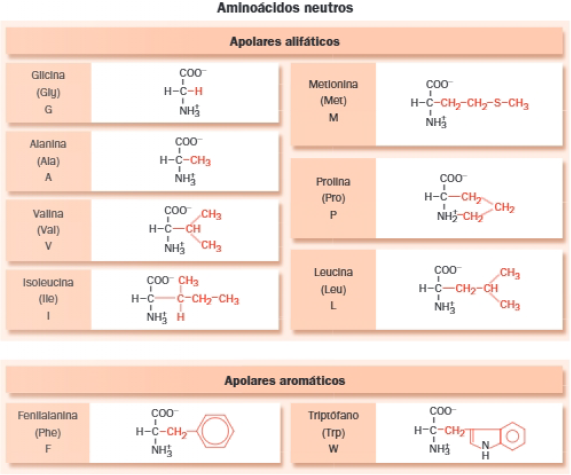
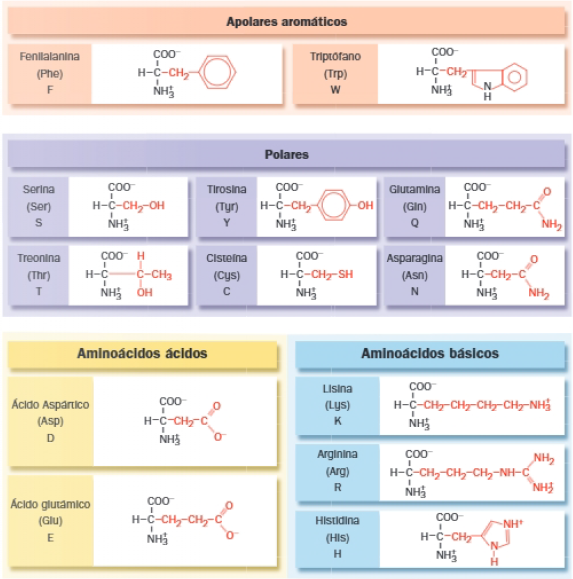
Propiedades de los aminoácidos
Los aminoácidos son moléculas de bajo peso molecular solubles al agua, cristalinos, incoloros y sólidos, ya que su punto de fusión es elevado y presentan actividad óptica y comportamiento anfótero.
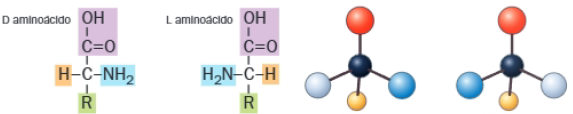
A. Esteroisomería
El carbono alfa de los aminoácidos, excepto la glicina, es un carbono asimétrico. Por ello, los aminoácidos pueden presentar dos configuraciones distintas: configuración L si el grupo -NH2 está a la izquierda y configuración D, si está a la derecha. Este mismo carbono determina que presenten actividad óptica y pueden ser dextrógiros (+) o levógiros (-), independientemente de su configuración L o D.
B. Carácter anfótero
En cada disolución acuosa, los aminoácidos muestran un comportamiento anfótero, es decir, actúan como ácidos o como bases según el pH de la disolución, ya que tienen un grupo carboxilo que puede ceder protones (hidrógeno) actuando como ácido y un grupo amino que puede captar protones (hidrógeno) actuando así como base.
Debio a este comportamiento, los aminoácidos mantienen constante el pH del medio, tienen efecto amortiguador o efecto tampón.
EL ENLACE PEPTÍDICO
El enlace peptídico es la forma de unión de los aminoácidos para formar polímeros.
Cuando reacciona el grupo carboxilo terminal de un aminoácido con el grupo amino terminal del siguiente aminoácido se forma un enlace peptídico y se desprende una molécula de agua.
Esta unión puede romperse por hidrólisis tanto física como enzimática
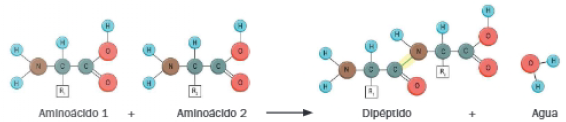
En el enlace peptídico, puesto que los cuatro átomos del enlace se sitúan en el mismo plano, son posibles dos configuraciones, cis y trans. El O del grupo carbonilo y el H del grupo amino normalmente están en lados opuestos del enlace, es decir, en configuración trans, que se ve favorecida para evitar interacciones entre los átomos. De la misma formas los radicales también se sitúan en lados alternos.
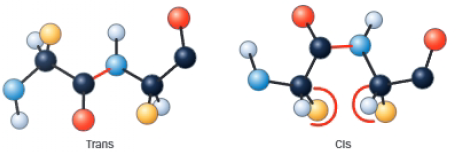
La disposición de los 6 átomos del enlace peptídico en el mismo plano le confiere carácter de doble enlace parcial, impidiendo la rotación. Este enlace está en un nivel intermedio entre sencillo y doble.
Características del enlace peptídico
El enlace peptídico es un enlace covalente tipo amida más corto que la mayoría de los demás enlaces N-C; como hemos visto, esto hace que tenga carácter parcial de doble enlace, lo que impide la rotación a su alrededor, así, los átomos del enlace peptídico se sitúan en el mismo plano manteniendo las distancias y los ángulos fijos.
Péptidos
Los péptidos son compuestos formados por la unión de aminoácidos mediante un enlace peptídico.
Según el número de aminoácidos que se unen hablamos de:
- Oligopéptido: con menos de 10 aminoácidos. En función del número de monómeros, hablamos de dipéptidos, tripéptido, tetrapéptidos, etc.
- Polipéptidos: de 10-100 aminoácidos.
- Proteínas: más de 100 aminoácidos.
Muchas sustancias naturales importantes son péptidos, es el caso de:
- Insulina: Hormona producida por el páncreas y que regula la concentración de glucosa en sangre, está formada por dos cadenas de 21y 30 aminoácidos unidas por puentes disulfuro.
- Glucagón: Hormona de 29 aminoácidos, actúan en el metabolismo del glucógeno liberando glucosas. Es la hormona antagónica de la insulina ya que, cuando el nivel de glucosa disminuye más de la cuenta en sangre, se libera esta hormona. Lo sintetizan las células alfa de los islotes de Langerhans del páncreas.
- Oxitocina: Hormona que es un péptido de 9 aminoácidos. Es una hormona relacionada con los patrones sexuales y las conductas maternal y paternal, actuando también como neurotransmisor del cerebro. La oxitocina se libera en el parto en grandes cantidades facilitando así las contracciones uterinas.
- Vasopresina: Hormona péptido también de 9 aminoácidos, solo difiere de la oxitocina en uno de ellos. Actúa sobre la musculatura disminuyendo la luz de los vasos sanguíneos.
- Endorfinas: Hormonas que son péptidos opioides que produce nuestro cuerpo y que funcionan como neutrotransmisores. Son producidas por la glándula pituitaria y el hipotálamo en vertebrados durante el ejercicio físico, cuando sentimos dolor o comemos determinados alimentos. Su efecto analgésico y la sensación de bienestar que producen han hecho que se les denomine hormonas de la felicidad.
- Antibióticos: como los decapéptidos, gramicidina y valinomicina.
- Venenos: encontramos péptidos que forman parte del escorpión y de la Amanita phalloides
ESTRUCTURA DE LAS PROTEÍNAS
Las proteínas son moléculas específicas que se sintetizan bajo las órdenes del ADN y son las responsables de las características y funciones de los seres vivos.
Las proteínas adoptan una determinada configuración espacial mediante plegamiento de las cadenas peptídicas que las forman, debido a las cargas que presentan los radicales libres de los aminoácidos que las forman y al enlace peptídico. Su función va a depender de esta disposición espacial.
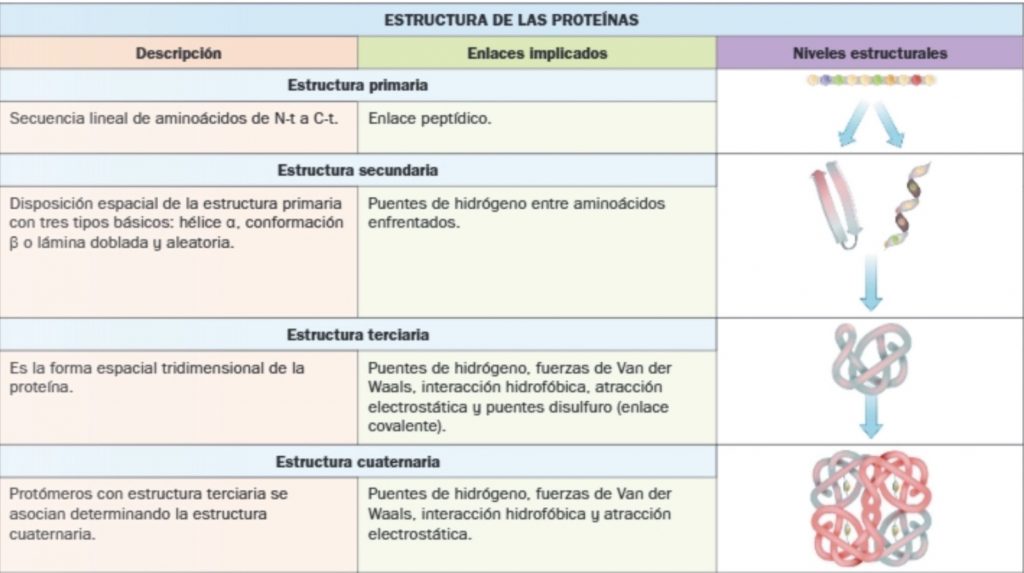
Estructura Primaria
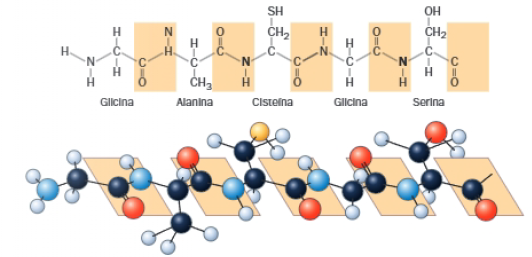
La estructura primaria es la secuencia lineal de aminoácidos que forman la proteína desde el extremo N-t (amino) al C-t (carboxilo).
De esta secuencia, determinada genéticamente, dependen el resto de niveles estructurales de la proteína y su función. De hecho, las proteínas estructurales como las que forman tendones y cartílagos tienen mayor cantidad de aminoácidos rígidos que establecen enlaces químicos fuertes unos con otros para dar dureza a la estructura que forman.
La estructura primaria se mantiene estable mediante un enlace peptídico entre los aminoácidos que la forman. El número de aminoácidos que forma esta cadena oscila entre 80 y 300.
Las chaperonas son proteínas presentes en todas las células, tanto procariotas como eucariotas, que contribuyen al correcto plegamiento proteico e intervienen en la proteólisis de proteínas mal plegadas. Muchas de ellas son proteínas de choque térmico (proteínas que producen las células sometidas a estrés).
Las chaperonas se unen a la estructura primaria de la proteína recién formada para ayudarla en su plegamiento, ensamblaje y transporte pero no forman parte de ella.
Estructura Secundaria
La estructura secundaria viene determinada por la disposición en el espacio de la estructura primaria anterior estabilizada por la formación de puentes de hidrógeno.
Los tipos más comunes de estructura secundaria son hélice alfa y conformación beta o lámina doblada.
- Hélice alfa: es la forma más simple y común. En este tipo de estructura la molécula adopta una disposición helicoidal, con giro a la derecha (dextógira) y con 3 a 4 aminoácidos por vuelta de espiral. Este tipo de organización es muy estable, porque permite la formación de puentes de hidrógeno entre el grupo C=O de un aminoácido y el grupo N-H del aminoácido con el que queda enfrentado; en total, se forman 7 enlaces por vuelta, lo que estabiliza enormemente la hélice. Las cadenas laterales de los aminoácidos se sitúan fuera del helicoide.
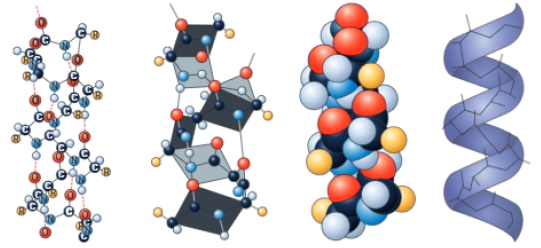
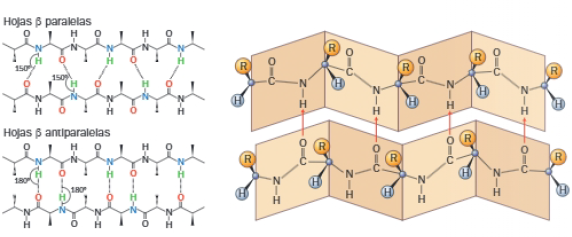
- Conformación beta o lámina doblada: en este caso, la cadena peptídica, o una parte de ella, adoptan una disposición en zigzag. Estas cadenas, que pueden pertenecer a péptidos diferentes o ser partes de una misma molécula, se sitúan adyacentes formando una lámina plegada como un acordeón. Si las cadenas se orientan en la misma dirección, hablamos de lámina paralela, si van en dirección contraria, lámina antiparalela.
La estructura se estabiliza por la formación de puentes de hidrógeno entre grupos C=O y hélice N-H de aminoácidos enfrentados. Las cadenas laterales van quedando alternativamente habia arriba y hacia abajo. La glicina y la alanina abundan en este tipo de estructuras.
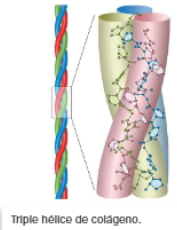
- Triple hélice de colágeno: un caso especial es la conformación de la proteína colágeno que forma una hélice peculiar debido a la abundancia de prolina en su estructura primaria. Presenta una secuencia típica compuesta por la repetición periódica de grupos de tres aminoácidos, siendo una glicina y dos prolinas.
Estructura Terciaria
La estructura terciaria aparece cuando la estructura secundaria de la proteína se dispone en el espacio formando una estructura tridimensional estable.
Esta estructura se denomina conformación nativa y la proteína ya es activa.
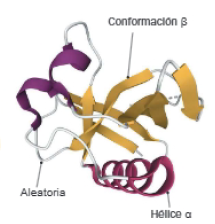
Presentará regiones con una estructura secundaria de hélice alfa, otras con conformación beta y zonas sin estructura definida asociada a puntos de flexión de la cadena, aleatorias. Los enlaces que estabilizan la estructura se forman entre las diferentes cadenas laterales de los aminoácidos que la forman y pueden ser: puentes de hidrógeno, interacción hidrofóbica, atracción electrostática, fuerzas de Van der Waals y puentes disulfuro. El puente disulfuro se establece entre cadenas laterales de cisteína, por su carácter covalente es la interacción más fuerte de cuantas estabilizan la estructura terciaria.
Distinguimos dos tipos de estructura terciaria:
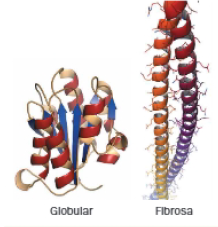
- Globular: se obtiene por plegamiento excesivo de la estructura secundaria. Por lo general, en los tramos rectos figuran hélices alfa y en los codos, estructuras sin definir.
Las cadenas laterales apolares se orientan hacia el interior de la molécula evitando las interacciones con el agua y las disoluciones salinas, mientras que las cadenas laterales polares se sitúan en la superficie de la molécula, interaccionan con el agua y las disoluciones salinas haciendo que la proteína sea soluble (ejemplo la mioglobina). - Fibrosa: el plegamiento de la estructura secundaria es escaso y se mantiene su estructura alargada. Son insolubles en agua y disoluciones salinas (ejemplo la elastina).
Estructura Cuaternaria
Las proteínas que realizan funciones de regulación del metabolismo celular suelen tener una estructura cuaternaria.
La estructura cuaternaria se forma cuando varias cadenas de aminoácidos, iguales o diferentes, que presentan un nivel estructural terciario (protómero) se unen entre sí y originan la proteína con estructura cuaternaria (oligómero).
La unión de una o varias proteínas a otras moléculas no proteicas para formar estructuras macromoleculares complejas también se considera una estructura cuaternaria.
Cuando estudiamos la estructura cuaternaria de la proteína debemos valorar lo siguiente:
- El número y la naturaleza de las distintas subunidades que forman el oligómero.
- La forma en que se asocian en el espacio para dar lugar al oligómero.
Los protómeros se mantienen unidos mediante enlaces no covalentes a otras subunidades proteicas; estos enlaces pueden ser: puentes de hidrógeno, fuerzas de Van de Waals, interacción hidrofóbica y atracción electrostática.
La estructura cuaternaria
Las proteínas que realizan funciones de regulación del metabolismo celular suelen tener una estructura cuaternaria.
La estructura cuaternaria presenta una serie de ventajas estructurales y funcionales: la economía genética y la eficiencia; sintetizamos protómeros y no proteínas completas, los protómeros son cadenas cortas, lo que requiere paquetes pequeños de información en el ADN; el trabajo es cooperativo, los protómeros trabajan juntos de manera coordinada, lo que supone una mayor eficacia y, además, las subunidades protoméricas se autoensamblan sin consumo energético formando estructuras complejas.
Según sea el número de protómeros que forman el complejo proteico hablamos de:
- Dímeros: formados por dos cadenas peptídicas, como la turbulenta que forma los microtúbulos celulares.
- Tetrámeros: formados por 4 cadenas peptídicas, como la hemoglobina que transporta oxígeno a la sangre.
- Pentámeros: formados por 5 cadenas peptídicas.
- Polímeros: formados por gran número de subunidades proteicas.
Por lo general, si se separan los protómeros de la estructura cuaternaria, no presentan actividad o se comportan de manera muy diferente a cómo lo hacen cuando están ensamblados.
PROPIEDADES DE LAS PROTEÍNAS
Las propiedades de las proteínas vienen determinadas por la estructura de estas.
Sus propiedades, al igual que su estructura, vienen determinadas por el tipo de radicales que presentan los aminoácidos que las forman y de su disponibilidad para reaccionar con otras moléculas.
Solubilidad
Las proteínas globulares son solubles mientras que las fibrosas son insolubles.
Como ya sabemos, las proteínas globulares son solubles al agua y disoluciones salinas pues los radicales libres de los aminoácidos que las forman, al ionizarse, establecen enlaces débiles por puentes e hidrógeno con las moléculas de agua.
La proteína soluble queda recubierta de una capa de moléculas de agua que impide que se pueda unir a otras proteínas y evita así su precipitación. Gracias a esta propiedad es posible la hidratación de los tejidos de los seres vivos.
El carátula insoluble de las proteínas fibrosas determinan que desempeñen funciones estructurales y no metabólicas.
Especificidad
Las proteínas son específicas. Esa especificidad no se refiere solo a su función, también hace referencia a que cada una de las especies de seres vivos fabrica sus propias proteínas, incluso individuos distintos de la misma especie presentan diferencias en sus proteínas.
Esta enorme especificidad explica los procesos de rechazo de órganos en los transplantes y en las transfusiones sanguíneas, procesos alérgicos y algunas infecciones.
La diversidad proteica interespecífica e intraespecífica se consigue por las múltiples combinaciones entre los aminoácidos proteicos, que está codificadas en el ADN de cada individuo.
Las proteínas que realizan la misma función en especies diferentes se llaman proteínas homólogas; cuanto más alejadas están filogenética mente dos especies, mayores son las diferencias entre estas proteínas. Comparando proteínas homólogas podemos determinar el grado de parentesco evolutivo entre individuos y construir árboles filogenéticos.
Comportamiento anfótero
Las proteínas tienen un comportamiento anfótero, por lo que son capaces de neutralizar las variaciones de pH del medio. Presentan, por lo tanto, una función homeostática.
Dependiendo de la naturaleza de los radicales libres de los aminoácidos que las forman podrán comportarse como un ácido o una base y, por tanto, liberar o retirar protones del medio donde se encuentran.
Desnaturalización
La conformación nativa de una proteína desaparece cuando se desnaturaliza, ya que se rompen los enlaces que mantienen su estructura cuaternaria, terciaria y secundaria y solo se conserva la estructura primaria, permaneciendo así solo los enlaces covalentes.
Las proteínas desnaturalizadas se transforman en filamentos lineales y delgados que se entrelazan hasta formar compuestos fibrosos e insolubles en agua. La pérdida de la conformación nativa proteica supone también la pérdida de su función biológica.
Los agentes que pueden desnaturalizar las proteínas son:
- Calor excesivo.
- Modificaciones del pH.
- Alteraciones en la concentración.
- Alta salinidad.
- Agitación molecular.
- Detergentes.
- Metales pesados.
- Urea.
- Radiaciones.
En determinadas condiciones, si los factores desnaturalizantes son poco intensos y breves en el tiempo, el proceso de desnaturalización puede volverse reversible, puesto que la proteína vuelve a su conformación nativa, es decir, la proteína se renaturaliza.
FUNCIONES DE LAS PROTEÍNAS
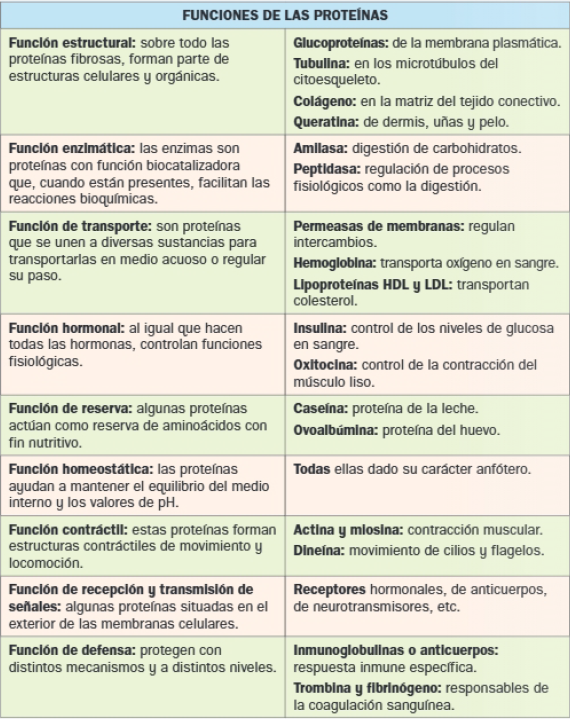
El grupo de las proteínas es muy abudante por lo que cabe esperar que lleven a cabo una gran diversidad de funciones.
En la siguiente tabla se recogen las principales funciones que desempeñan, así como algunos ejemplos de las mismas:
CLASIFICACIÓN DE LAS PROTEÍNAS
La clasificación de las proteínas es compleja, dada la enorme diversidad estructural y funcional de eta biomolécula.
Utilizando como criterio de clasificación la composición química, hablamos de proteínas simples, holoproteínas y conjugadas, heteroproteínas.
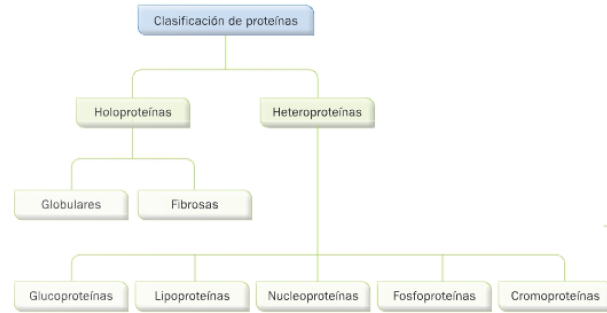
Holoproteínas o proteínas simples
Las holoproteínas están constituidas únicamente por una o varias cadenas de aminoácidos. Distinguimos, según su configuración, dos grupos:
- Proteínas globulares o esferoproteínas: Presentan generalmente conformación esférica u ovoide, son compactas, con muchas uniones entre sí y gran actividad biológica, y, como habíamos visto, son solubles al agua y disoluciones salinas, encontrando tres tipos a su vez, que son las globulinas, albúminas y la activa G.
- Proteínas fibrosas o escleroproteínas: Con estructura sencilla, como ya vimos, son insolubles y tienen una función principalmente estructural, distinguiendo entre ellas a la miosina, queratina, elastina y el colágeno.
Heteroproteínas o proteínas conjugadas
Las heteroproteínas contienen además de aminoácidos otro compuesto de naturaleza no proteica que se denomina grupo prostético.
Según la naturaleza química de este grupo, las clasificamos en las siguientes:
- Glucoproteínas: Su grupo prostético es un glúcido (inmunoglobulinas).
- Lipoproteínas: Su grupo prostético es un lípido (HDL, LDL).
- Nucleoproteínas: Su grupo prostético es el ADN (cromatina).
- Fosfoproteínas: Su grupo prostético es el ácido fosfórico (caseína).
- Cromoproteínas: Su grupo prostético es una sustancia coloreada o pigmento (hemocianina, citocromos).
Fuente: Biología 2 (Mc Graw Hill)