
INTRODUCCIÓN AL METABOLISMO
Las células son sistemas abiertos que intercambian materia y energía con su retorno. Toman del medio materia y energía, y la transforman en materia propia y en formas de energía utilizables para el mantenimiento de la vida.
En el interior de las células tienen lugar, de modo simultáneo y perfectamente coordinado, infinidad de reacciones químicas.
El metabolismo puede definirse como el conjunto de procesos químicos catalizados por enzimas que tienen lugar en el interior de las células.
Los principales objetivos del metabolismo son:
- Transformar las sustancias incorporadas del entorno en materia prima para la célula.
- Obtener energía utilizable para las células (ATP).
- Fabricar y reparar los componentes celulares.
- Fabricar y degradar moléculas con funciones específicas (hormonas, neurotransmisores, etc.).
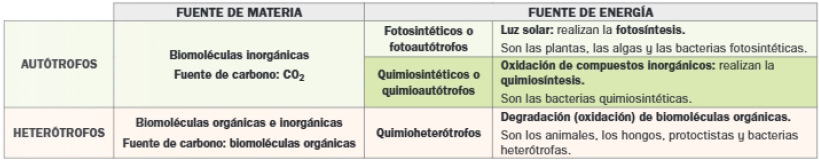
Metabolismo autótrofo y heterótrofo
Se distinguen dos modalidades de metabolismo en función de la fuente de materia y de energía utilizadas, que permite clasificar a los organismos y/o las células en función de ellas.
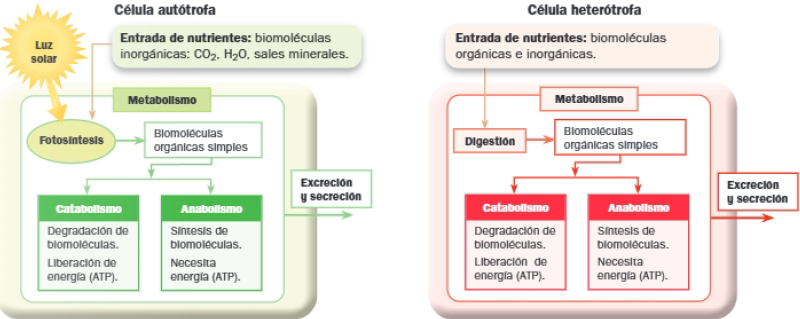
Catabolismo y anabolismo
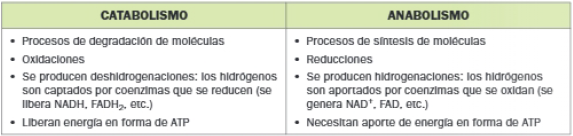
Las reacciones químicas que constituyen el metabolismo se pueden agrupar en dos tipos de procesos: catabólicos y anabólicos.
- Procesos catabólicos: implican la degradación de moléculas complejas a otras más simples. Se trata de procesos de oxidación, en los que las moléculas ceden hidrógenos y en los que se libera energía.
- Procesos anabólicos: en ellos se produce la síntesis de moléculas complejas a partir de otras más sencillas; se trata de reducciones en las que las moléculas captan hidrógenos, consumiendo energía.
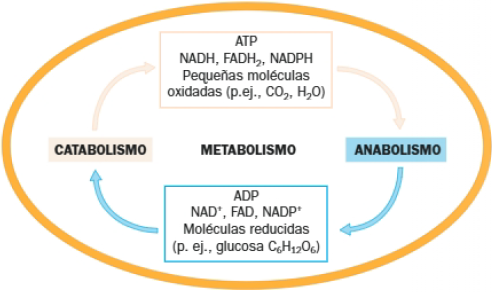
A. Reacciones de oxidación-reducción
Las reacciones del metabolismo son de oxidación-reducción; en muchas reacciones metabólicas la oxidación equivale a la deshidrogenación (se pierden electrones y protones en forma de átomos de hidrógeno) y la reducción a la hidrogenación (ganancia de átomos de hidrógeno). Las moléculas se reducen, por tanto, captando hidrógenos y se oxidan cuando los ceden.
De modo general, los procesos catabólicos son oxidaciones y los anabólicos, reducciones.
Determinadas coenzimas actúan como intermediarias entre las reacciones de oxidación y las de reducción, debido a su facilidad para captar o ceder hidrógenos. Las principales son:
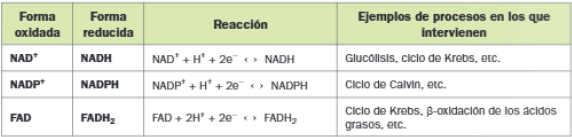
B. El ATP y los intercambios de energía
Los procesos que liberan energía y los que la necesitan de modo simultáneo ni en el mismo lugar de la célula. Pero existen mecanismos que transportan esa energía desde los puntos donde se libera a los que la necesitan.
El mecanismo de transferencia de energía más utilizado por las células es el denominado ciclo del ATP-ADP, que implica la formación y rotura de enlaces ricos en energía entre los grupos fosfato 2 y 3 del ATP.
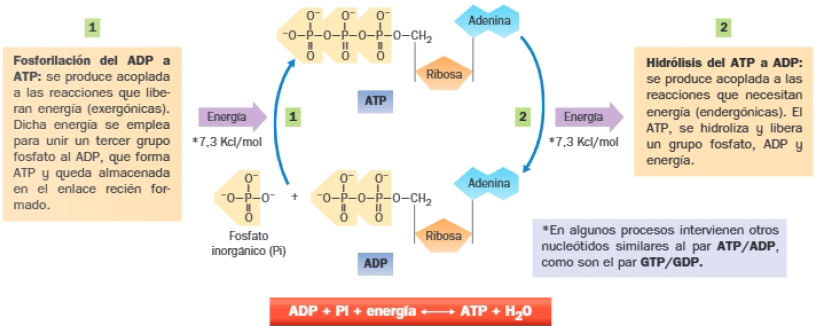
¿Donde se sintetiza el ATP?
Las células utilizan dos mecanismos de síntesis de ATP: la fosforilación a nivel de sustrato y la fosforilación por las ATPasas o ATP sintasas.
- Fosforilación a nivel de substrato: En este caso, un compuesto rico en energía se hidroliza y la energía liberada es utilizada para fosforilar el ADP a ATP. El grupo fosfato puede ser cedido por una molécula orgánica fosforilada o puede tratarse de fosfato inorgánico presente en el medio.
- Fosforilación por las ATP sintasas: Se produce en mitocondrias y en cloroplastos, asociada al transporte de electrones a través de cadenas de transportadores situados en la membrana mitocondrial interna y en las membranas tilacoidales de los cloroplastos. El flujo de electrones libera energía utilizada para generar un gradiente electroquímico de H+, que será el que active las ATP sintasas.
- Si la síntesis ocurre en las ATPasas de las mitocondrias, durante la respiración celular, se trata de la fosforilación oxidativa.
- Si la síntesis ocurre en las ATPasas de los cloroplastos, durante la fotosíntesis, se denomina fosforilación.
Reacciones y rutas metabólicas
Las reacciones metabólicas poseen una serie de características que citaremos a continuación:
- Los reactivos y los productos se encuentran disueltos en agua. El agua, además, puede actuar también como reactivo o como producto de numerosas reacciones metabólicas.
- Todas las reacciones están catalizadas por enzimas.
- Son secuenciales, es decir, se organizan en rutas o vías metabólicas: secuencias de reacciones en las que el producto de una es el sustrato de la siguiente.
- En una ruta metabólica diferenciamos: el sustrato inicial, los metabolitos intermedios y el producto final.
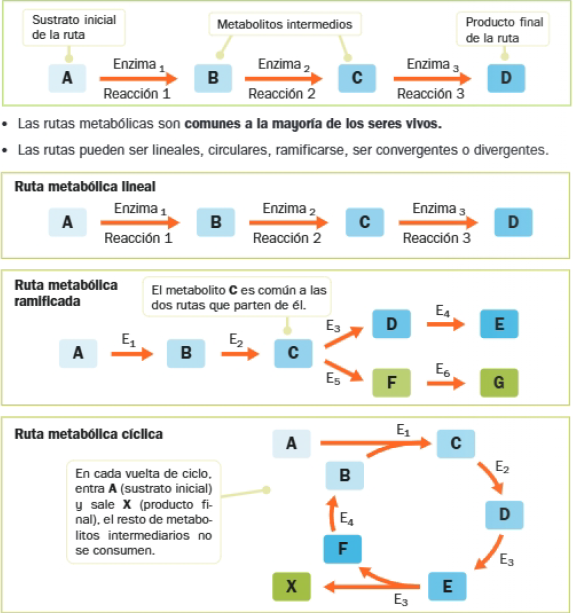
LAS ENZIMAS
Sin las enzimas, el metabolismo no sería posible. Gracias a su acción catalizadora tienen lugar en las células reacciones que, sin ellas, requerirían condiciones inviables de presión, temperatura o pH.
Los catalizadores son sustancias capaces de acelerar (catalizador positivo) o retardar (catalizador negativo) una reacción química, sin consumirse durante la reacción, es decir, el catalizador permanece inalterado al final del proceso.
Las enzimas son biocatalizadores positivos (aceleran), proteínas globulares que catalizan reacciones químicas en los seres vivos, y facilitan y aceleran dichas reacciones.
Las enzimas logran que la velocidad de las reacciones se adapte a las necesidades de los organismos en cada momento, de modo que los procesos metabólicos tienen lugar de forma ordenada y eficaz.
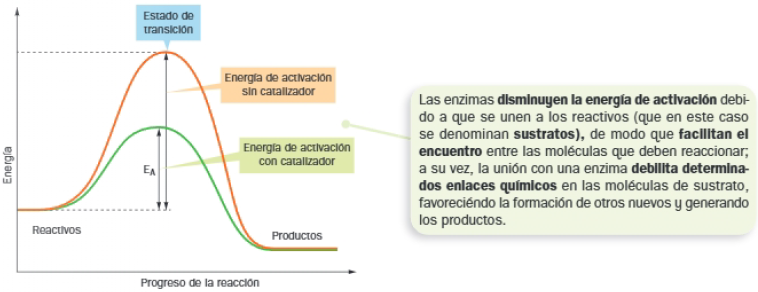
Las enzimas disminuyen la energía de activación
Para que se produzca una reacción química, sea endotérmica o exotérmica, es necesario que las moléculas que van a reaccionar o reactivos alcancen el denominado estado de transición, en el cual los reactivos se encuentran y determinados enlaces se vuelven inestables, rompiéndose y formándose otros nuevos para originar los productos.
Para llevar a los reactivos al estado de transición, se requiere un aporte energético inicial o energía de activación.
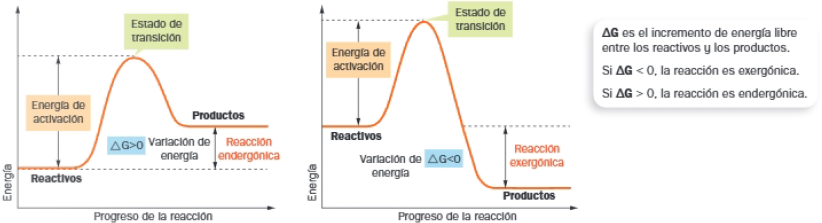
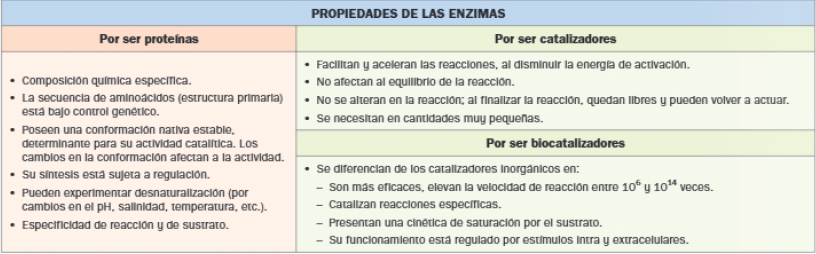
Propiedades de las enzimas
Las enzimas poseen propiedades derivadas de su naturaleza proteica y del hecho de ser catalizadores de las reacciones químicas de los seres vivos.
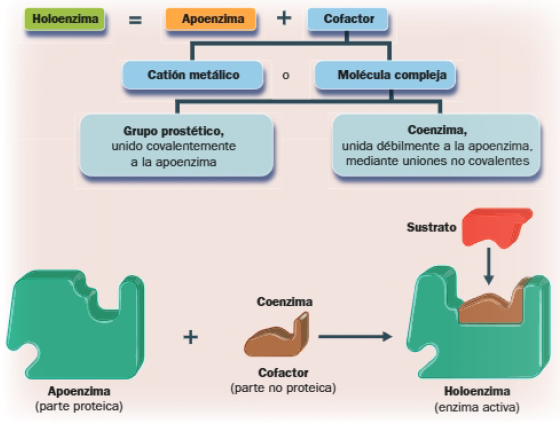
Naturaleza química de las enzimas
Las enzimas son proteínas globulares. En función de su composición, se diferencian:
- Enzimas sencillas: son proteínas, compuestas exclusivamente por una o más cadenas de aminoácidos.
- Enzimas conjugadas o holoenzimas: constan de una parte proteica, la apoenzima, y una parte no proteica, el cofactor.
El cofactor puede ser una catión metálico o una molécula compleja; en este caso, si está unida covalentemente a la apoenzima, se denomina grupo prostético y, si la unión es débil, transitoria, se conoce como coenzima.
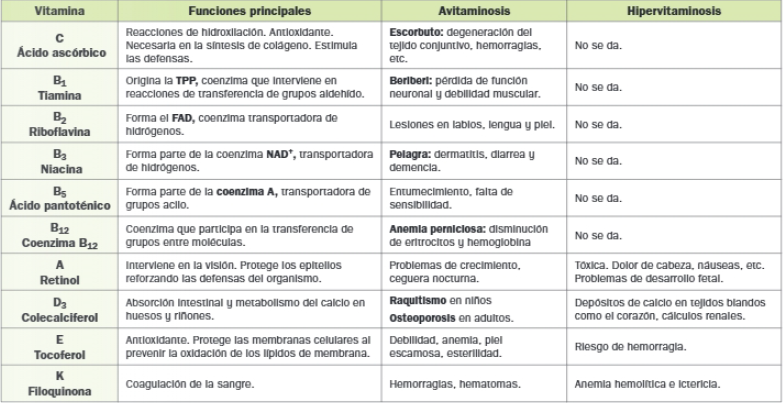
Vitaminas y coenzimas
Las vitaminas son un grupo de compuestos de naturaleza muy variada, la mayoría de las cuales actúan como coenzimas y grupos prostéticos de las enzimas. Sin las coenzimas y grupos prostéticos, no es posible la activación de numerosas enzimas; por lo tanto, las vitaminas resultan imprescindibles.
Las vitaminas realmente son moléculas orgánicas heterogéneas, que se requieren en pequeñas cantidades para el mantenimiento de las funciones metabólicas, pero que no pueden ser sintetizadas por el organismo en cantidades adecuadas, por ello, deben incluirse en la dieta.
Su defecto (avitaminosis) como se exceso (hipervitaminosis) causan enfermedades.
Clasificación de las vitaminas
Las vitaminas se clasifican en dos grupos, en función de su solubilidad:
- Vitaminas hidrosolubles: solubles al agua; no se almacenan, el exceso se elimina a través de la orina, por lo que deben reponerse con regularidad. Son las vitaminas C y el grupo B.
- Vitaminas liposolubles: solubles en grasas. Se pueden almacenar en el organismo (hígado y tejido adiposo), por lo que el exceso puede resultar tóxico. Son A, D, E y K.
Mecanismo de acción enzimática
Las enzimas actúan sobre sustancias denominadas sustratos, que se unen a la enzima en un lugar concreto denominado centro o sitio activo; la unión del sustrato a la enzima genera el complejo enzima-sustrato. Las enzimas facilitan que los sustratos se sitúen con la orientación óptima para que la reacción se produzca. La unión al centro activo de la enzima lleva al sustrato al estado de transición, de modo que determinados enlaces se vuelven inestables y se forman otros nuevos, que originan los productos; al finalizar la reacción, el producto se separa de la enzima. La enzima libre puede actuar de nuevo.
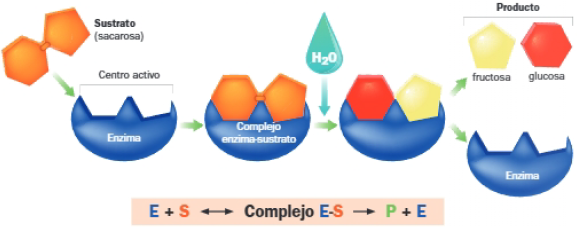
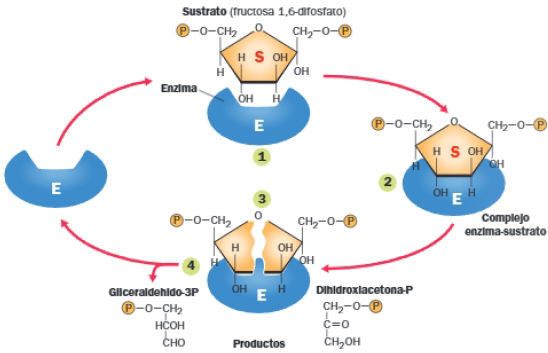
A. La especificidad enzimática
El centro activo es el lugar de la enzima al que se une el sustrato y donde tiene lugar la catálisis. Es el responsable de la actividad catalítica de la enzima y de su especificidad.
Existe una especificidad de sustrato: al centro activo solo puede unirse un sustrato concreto. Y una especificidad de acción: cada enzima realiza un tipo de transformación, de reacción sobre el sustrato.
La especificidad de sustrato puede presentar diferentes niveles:
- Absoluta: la enzima solo actúa sobre un sustrato.
- De grupo: la enzima reconoce un grupo funcional a varios sustratos.
- Estereoquímica: la enzima selecciona incluso los distintos isómeros de un sustrato.
B. Modelos de interacción enzima-sustrato
Para explicar la unión del sustrato a la enzima se han propuesto básicamente dos modelos: el modelo de llave-cerradura y el de ajuste inducido o guante-mano.
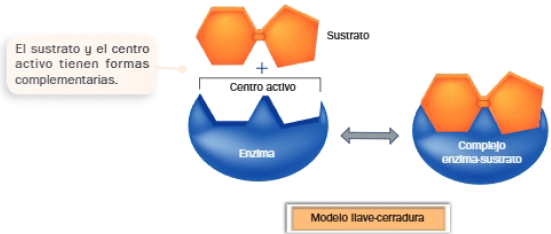
Modelo de Fishcher (1894) o de llave-cerradura
Según este primer modelo de interacción entre el sustrato y la enzima, la estructura del sustrato y la del centro activo serían complementarias; el sustrato encajaría en el centro activo del mismo modo que una llave encaja en la cerradura correspondiente.
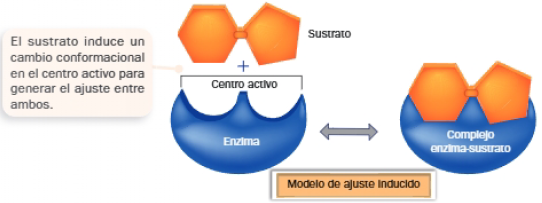
Modelo de Koshland (1958) de ajuste inducido o guante-mano
Según este nuevo modelo, el centro activo adopta la conformación espacial idónea solo en presencia del sustrato. La unión sustrato-centro activo desencadena un cambio conformacional, de modo similar a cómo la mano induce la adaptación del guante a su forma.
Factores que condicionan la actividad enzimática
Existen numerosos factores que influyen en la actividad de las enzimas; entre ellos: la concentración de sustrato, el pH, la temperatura y la presencia de inhibidores y activadores.
A. Efecto de la concentración de sustrato
Leonor Michaells y Maud Menten determinaron la influencia de la concentración de sustrato en la velocidad de las reacciones catalizadas por enzimas; es la denominada cinética de Michaells-Menten.
En determinadas condiciones, manteniendo constante la temperatura y la concentración de enzima, al incrementar la concentración de sustrato, se obtiene energía gráfica:
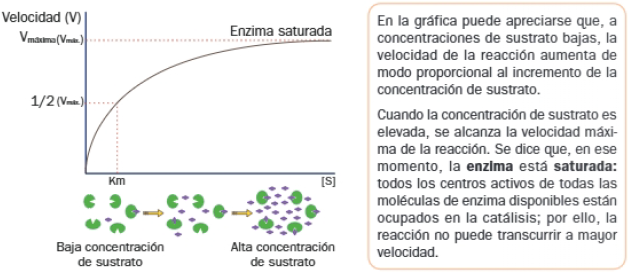

Significado biológico de la Km de una enzima
La Km es característica de cada enzima. La Km de una enzima indica cuánto sustrato necesita para alcanzar la mitad de su velocidad máxima, por lo tanto, es indicativa del grado de afinidad de la enzima por el sustrato:
- Una Km baja indica una gran afinidad de la enzima por el sustrato; con muy poco sustrato, la velocidad se incrementa notablemente.
- Una Km alta indica escasa afinidad de la enzima por el sustrato; necesita una elevada concentración de sustrato para que se forme el complejo enzima-sustrato.
B. Efecto del pH
Las enzimas son proteínas globulares, tienen una conformación espacial que depende de las interacciones entre los grupos R de los aminoácidos que la integran. La acción catalítica está directamente vinculada a su estructura tridimensional. La pérdida de esta estructura tridimensional, o conformación nativa, supone la pérdida de la actividad enzimática.
El pH del medio altera los grupos R de los aminoácidos y, por tanto, el plegamiento de la proteína y su actividad.
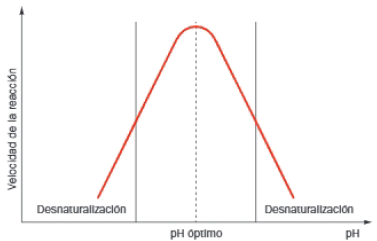
Para cada enzima existe un pH óptimo en el que la conformación espacial de la proteína es la óptima para su acción catalítica; a este pH la velocidad de la reacción enzimática será máxima.
Desviaciones de pocas décimas del pH óptimo, pueden disminuir drásticamente la actividad de una enzima. Existe además un pH máximo y un pH mínimo que delimitan el intervalo de pH en el que la enzima se mantiene activa. Si el pH del medio supera el pH máximo o desciende por debajo del pH mínimo, la enzima se desnaturaliza y, por tanto, se inactiva. Por este motivo, resultan imprescindibles los sistemas tampón que regulan el pH en los organismos vivos.
C. Efecto de la temperatura
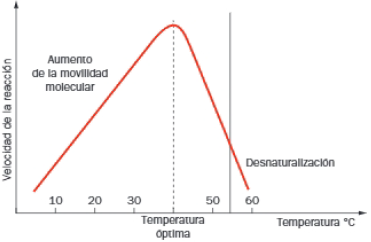
En general, la velocidad de las reacciones químicas aumenta con la temperatura, por cada 10 grados centígrados de incremento de la temperatura, la velocidad de la reacción se duplica. En las reacciones catalizadas por enzimas, esto solo es posible hasta una temperatura «crítica» que se corresponde con la temperatura óptima, en la que la enzima alcanza la máxima velocidad de reacción.
Si se supera la temperatura óptima, la actividad enzimática sufre un descenso brusco, debido a que se produce la desnaturalización de la proteína.
La temperatura crítica de la mayoría de las enzimas oscila entre los 55-60 grados centígrados, pero las enzimas de las arqueobacterias extremófilas, que viven en aguas termales, llegan a poseer temperaturas críticas de 80-87 grados centígrados.
D. Presencia de inhibidores y activadores
Las necesidades de las células son cambiantes y las reacciones químicas que tienen lugar en ellas deben responder a dichas necesidades; por lo tanto, resulta imprescindible regular la actividad de las enzimas, de modo que permanezcan activas solo aquellas que deban actuar en cada momento, para evitar la acumulación de productos innecesarios.
El pH y la temperatura tienen efectos en la actividad enzimática, pero no pueden utilizarse para regularla, puesto que sus valores se mantienen constantes en los organismos para preservar la estabilidad de numerosas biomoléculas.
Para regular la actividad enzimática, los organismos utilizan inhibidores y activadores; además de mecanismos como el alosterismo.
Inhibición enzimática
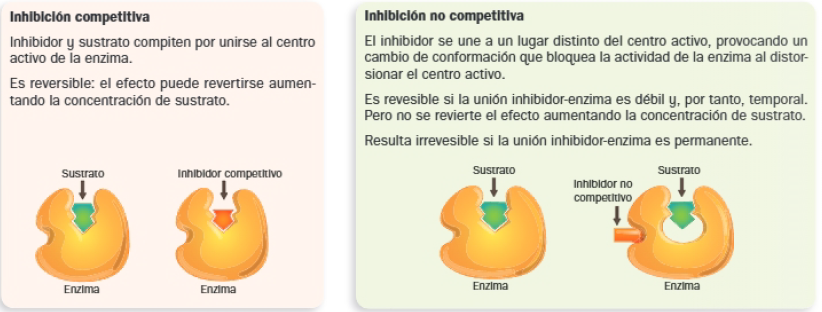
Activación enzimática
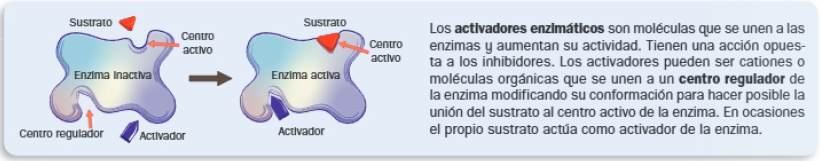
E. Enzimas alostéricas
Las enzimas alostéricas son enzimas reguladoras que presentan las siguientes características:
- Puede adoptar dos conformaciones interconvertibles llamadas conformación R (relajada) y conformación T (tensa). La R es muy activa, con una alta afinidad por el sustrato y la T es inactiva.
- Poseen centros reguladores, a los que pueden unirse moléculas moduladoras o efectoras, que pueden ser inhibidoras o activadoras. Las inhibidoras estabilizan la forma T y las activadoras la forma R.
- En general, poseen varias subunidades, varias cadenas peptídicas. Entre las subunidades se da un efecto cooperativo: la unión de un activador o un inhibidor a una de las subunidades induce la activación o inhibición de las demás.
- Presentan una cinética diferente a las enzimas no alostéricas, en relación con la concentración de sustrato; la gráfica es una curva sigmoidea:
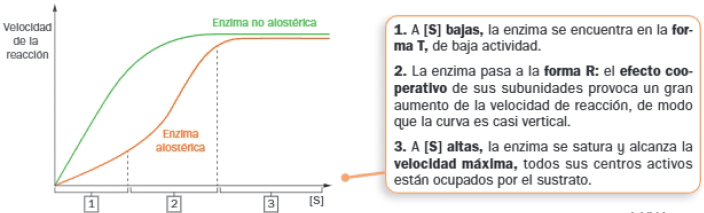
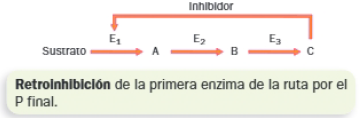
Las enzimas reguladoras se sitúan en el inicio de rutas metabólicas y en las ramificaciones de las mismas, para activar, detener u orientar los proceso según las necesidades de las células. La primera enzima de una ruta metabólica suele ser una enzima alostérica, para la cual, el sustrato inicial actúa como activador y el producto final como inhibidor, proceso denominado retroinhibición.
Clasificación de las enzimas
Las enzimas se agrupan en seis clases principales, en función del tipo de reacción que catalizan. Estas clases son:
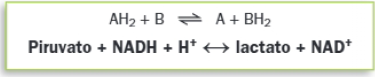
Clase 1: Oxidorreductasas. Catalizan reacciones de oxidación-reducción, con pérdida o ganancia de electrones. Las más características son las deshidrogenasas, que transfieren los hidrógenos a coenzimas como FAD, NAD+ o NADP+.
Clase 2: Transferasas. Catalizan la transferencia de grupos funcionales.

Clase 3: Hidrolasas. Catalizan reacciones por hidrólisis, en las que se rompen diferentes tipos de enlaces por adición de agua.

Por ejemplo, las lipasas rompen enlaces éster, la sacarasa, la lactasa o la amilasa rompen enlaces glucosídicos y las peptidasas, enlaces peptídicos.
Clase 4: Llasas. Catalizan la adición o eliminación de grupos funcionales.

Por ejemplo, las carboxilasas y descarboxilasas adicionan o eliminan CO2. El rubisco es la enzima más abundante de la naturaleza; cataliza la fijación de CO2 en la rubilosa 1,5-difosfato durante la fase oscura de la fotosíntesis.
Las amilasas y desaminasas adicionan o eliminan grupos amino.

Clase 5: Isomerasas. Catalizan la interconversión de isómeros.

Clase 6: Ligasas o sintetasas. Catalizan la unión de dos sustratos, acoplada a la hidrólisis simultánea de un nucleótido trifosfato.

Fuente: Biología 2 (Mc Graw Hill).